Les premières études épidémiologiques chinoises publiées après l’épidémie asiatique ont mis en évidence une association entre les comorbidités cardiovasculaires et la morbi-mortalité liée au COVID-19(1,2). Compte tenu de la propagation rapide et mondiale du SARS-CoV-2, et sur la base des caractéristiques de la maladie COVID-19 actuellement observées, les spécialistes des maladies cardiovasculaires sont et resteront activement engagés dans la prise en charge de ces patients pour de nombreuses raisons. Tout d’abord, parce qu’une maladie cardiovasculaire préexistante peut prédisposer à une infection SARS-CoV-2. Ces patients atteints de maladies cardiovasculaires, s’ils sont infectés par le SARS-CoV-2, présentent un risque élevé de formes graves et de complications(2-4). Enfin, les traitements proposés pour traiter le COVID-19 peuvent avoir des effets secondaires sur le système cardiovasculaire. Les soignants, à risque de contracter le virus, sont aussi des vecteurs de transmission du virus à leurs patients fragiles porteurs de pathologies cardiovasculaires chroniques et à risque de décompensation.
L’objectif de cette revue est de caractériser l’impact cardiovasculaire du COVID-19, ses conséquences potentielles chez les patients atteints d’une pathologie cardiovasculaire préexistante, ainsi que les impacts potentiels collatéraux chez tous les patients (avec ou sans COVID-19), et le personnel soignant.
Prévalence des maladies cardiovasculaires chez les patients COVID-19
Les maladies cardiovasculaires (MCV) avaient déjà été décrites comme comorbidité fréquente chez les patients atteints des 2 coronavirus ayant précédé le SARS-CoV-2, le SARS-CoV et le MERS-CoV. Dans le cas du SARS-CoV-2, la prévalence du diabète et des MCV était respectivement de 11 % et 8 %, et la présence de l’une ou l’autre de ces comorbidités multipliait par 12 le risque de décès(2,5). De nombreux éléments ont compliqué les efforts pour estimer la prévalence des MCV chez les patients atteints de COVID-19 : absence de tests généralisés, de surveillance nationale et de collecte de données standardisées ; biais d’échantillonnage chez les patients hospitalisés présentant des comorbidités plus nombreuses (notamment MCV) ; variations des méthodes utilisées par différents pays. Certaines études suggèrent une association entre les MCV préexistantes et les formes graves de COVID-19 (tableaux 1 et 2). Une métaanalyse de six études portant sur 1 527 patients COVID-19 a retrouvé des prévalences d’hypertension, de maladies cardiaques et cérébro-vasculaires, et de diabète de 17,1 %, 16,4 % et 9,7 %, respectivement(3). Les patients admis en soins intensifs avaient plus souvent des MCV.
Dans l’analyse de 44 672 cas confirmés de COVID-19 à Wuhan, les taux de mortalité étaient plus importants chez les patients atteints de MCV (10,5 %), de diabète (7,3 %), ou d’hypertension (6,0 %) que dans la population globale (2,3 %)(6). Plusieurs études de cohortes plus petites ont rapporté des résultats similaires(1,7). Bien que les données en dehors de la Chine soient encore limitées, les résultats italiens montrent également un risque élevé de décès chez les patients avec des comorbidités(8).
Les mécanismes sous-tendant ces associations restent peu clairs. Parmi les explications possibles, on peut citer le fait que les MCV deviennent plus fréquentes avec l’âge, sur un système immunitaire fonctionnellement affaibli, avec des niveaux élevés d’angioconvertase de type 2 (ACE2).
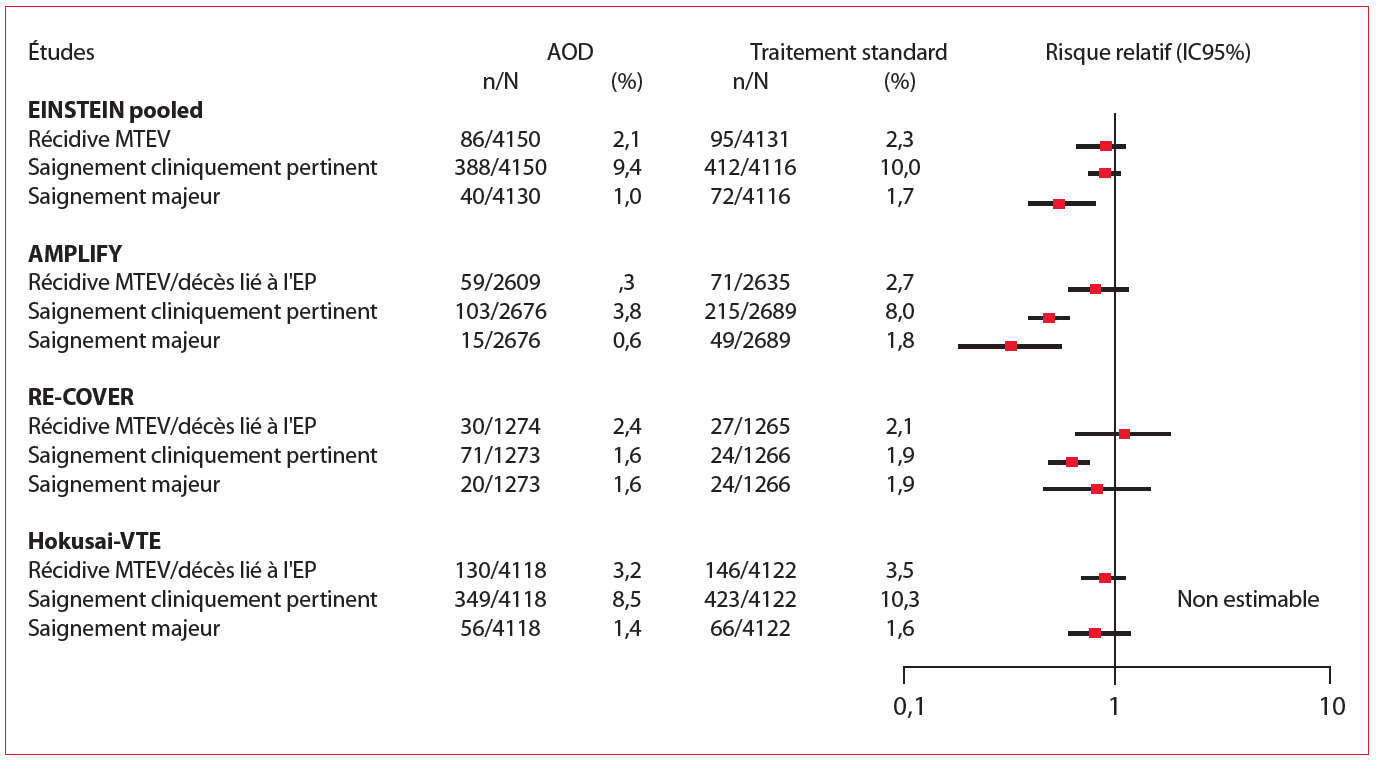
Tableau 1. Fréquence relative des facteurs de risque cardiovasculaire et des pathologies cardiovasculaires préexistantes chez les patients COVID-19.
D’après Driggin E et al. Cardiovascular considerations for patients, health care workers, and health systems during the coronavirus disease 2019 (COVID-19) pandemic. JACC mars 2020
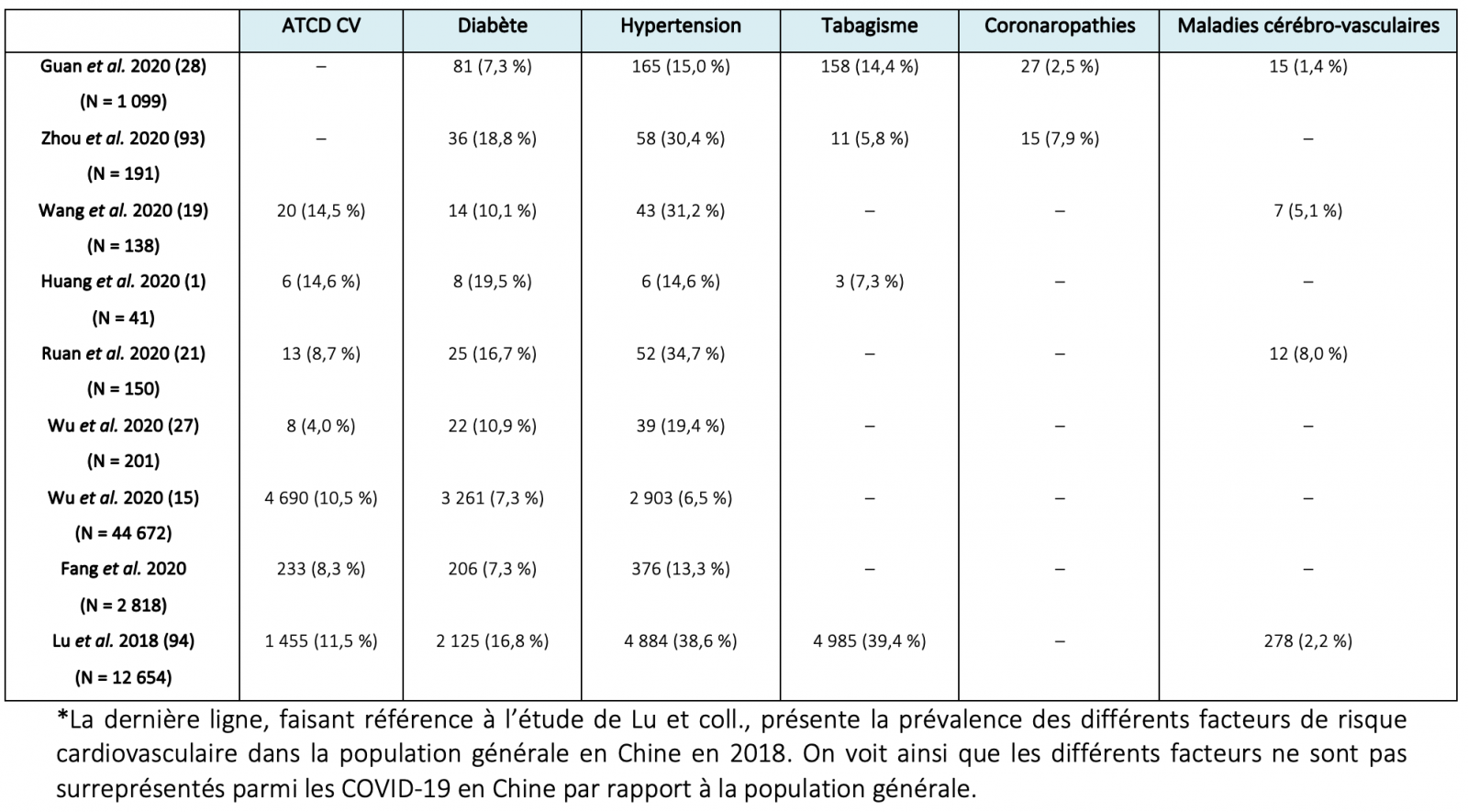
Tableau 2. Fréquence relative des facteurs de risque cardiovasculaires et des pathologies cardiovasculaires préexistantes chez les patients atteints du COVID-19 en fonction de la gravité du COVID (soins intensifs versus pas de soins intensifs).
D’après Driggin E et al. Cardiovascular considerations for patients, health care workers, and health systems during the coronavirus disease 2019 (COVID-19) pandemic. JACC mars 2020
Liens COVID-19 et maladies cardiovasculaires : mécanismes potentiels
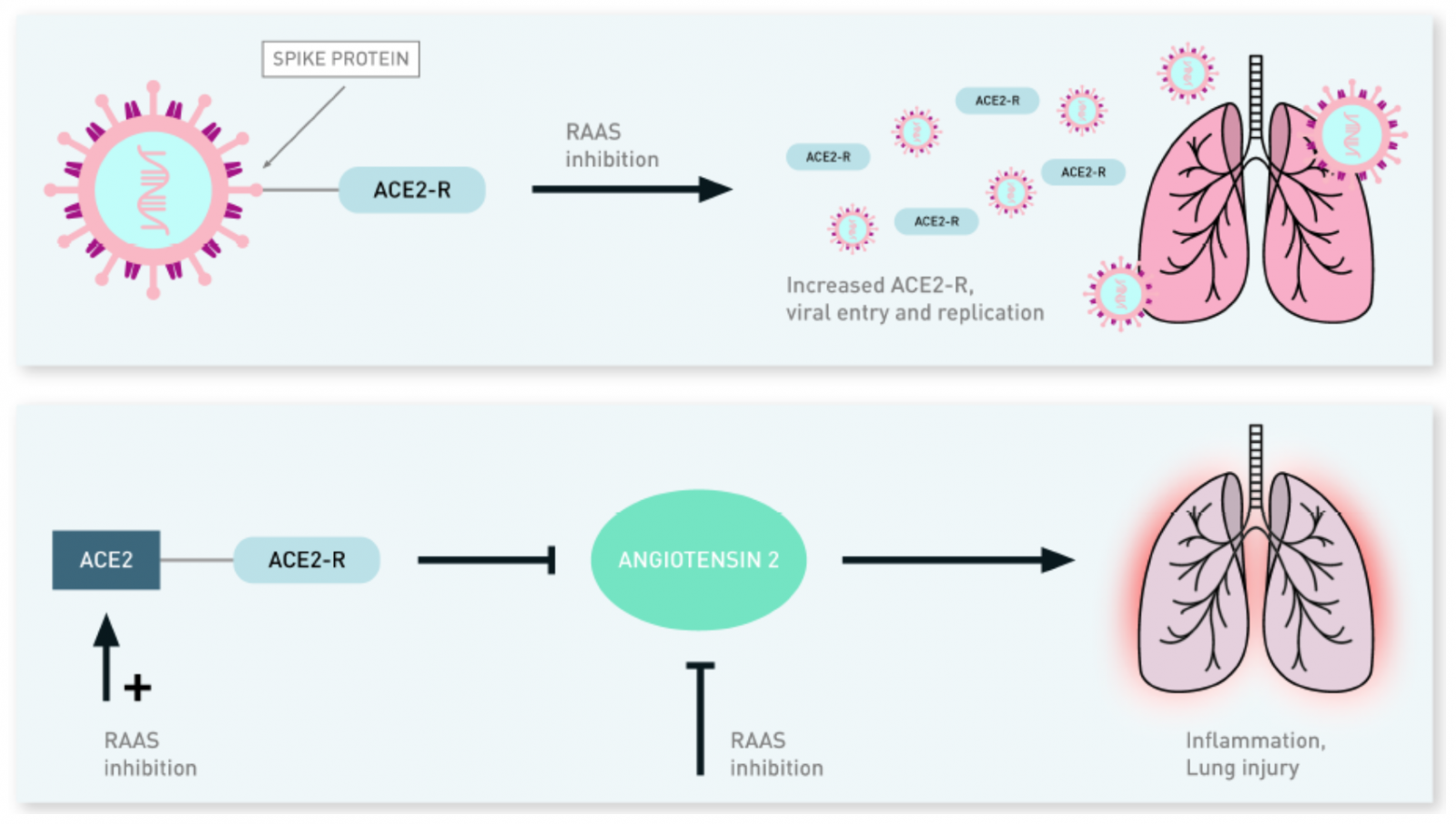
Il est de plus en plus admis que les mécanismes qui conduisent aux maladies cardiovasculaires impliquent les voies de régulation des fonctions immunitaires. L’effet de l’âge sur le système immunitaire est illustré par des titres faibles d’anticorps chez 50 % des adultes de plus de 65 ans qui reçoivent le vaccin contre la grippe saisonnière(9). D’autres facteurs de risque traditionnels de MCV (diabète, dyslipidémie) ont un impact sur les fonctions immunitaires et, inversement, un statut immunologique défaillant est associé à un risque élevé d’événement cardiovasculaire(10,11). Les pathologies cardiovasculaires peuvent être le marqueur d’une forme de vieillissement/dérèglement du système immunitaire, indirectement liées au pronostic du COVID-19. Une augmentation des événements cardiovasculaires après une infection par SARS-CoV-2 pourrait également jouer un rôle dans le pronostic, comme pour d’autres infections virales telles que la grippe(12,13). L’infection par SARS-CoV-2 peut activer des voies de signalisation qui lui sont propres et qui contribuent au plus mauvais pronostic chez les patients atteints de MCV. Par exemple, une expression plus élevée d’ACE2 chez les patients atteints d’hypertension artérielle et de MCV pourrait accroître la sensibilité au SARS-CoV-2, bien que les données sur le sujet soient contradictoires (figure 1)(14,15). Le SARS-CoV2 ainsi que d’autres coronavirus peuvent utiliser l’ACE2 comme récepteur pour sa pénétration dans la cellule infectée. L’ACE2 est une protéine transmembranaire de type I impliquée dans la boucle de contre-régulation du système rénine angiotensine. Elle est fortement exprimée dans les cellules alvéolaires pulmonaires, qui constituent le principal site d’entrée du virus chez l’homme(16). Après sa liaison à l’ACE2, le SARS-CoV-2 pénètre dans les cellules par endocytose. L’ACE2 joue un rôle protecteur au niveau pulmonaire, et de ce fait, la liaison du virus à l’ACE2 qui en diminue la disponibilité à la surface de la cellule hôte, contribuerait à la pathogénicité virale sur le système rénine angiotensine(17) (figure 1).
D’après la littérature chinoise disponible, et les premiers articles italiens, les facteurs de risque cardiovasculaire ne semblent pas surreprésentés chez les patients COVID-19 par rapport à la population générale. Par contre, les facteurs de risque cardiovasculaire, y compris un antécédent de MCV, exposent à une surmortalité(2,3,5,6,8).
Il est intéressant de noter qu’en ce qui concerne le tabac, contrairement à ce que l’on aurait pu attendre concernant un virus à tropisme respiratoire dont la manifestation grave est une pneumopathie sévère avec syndrome de détresse respiratoire aiguë (SDRA), la prévalence du tabagisme actif est beaucoup plus basse chez les COVID (entre 5 et 14 %), que dans la population générale chinoise où elle est particulièrement élevée à 40 % (tableau 1). Une théorie selon laquelle la nicotine pourrait avoir un effet protecteur est actuellement explorée.
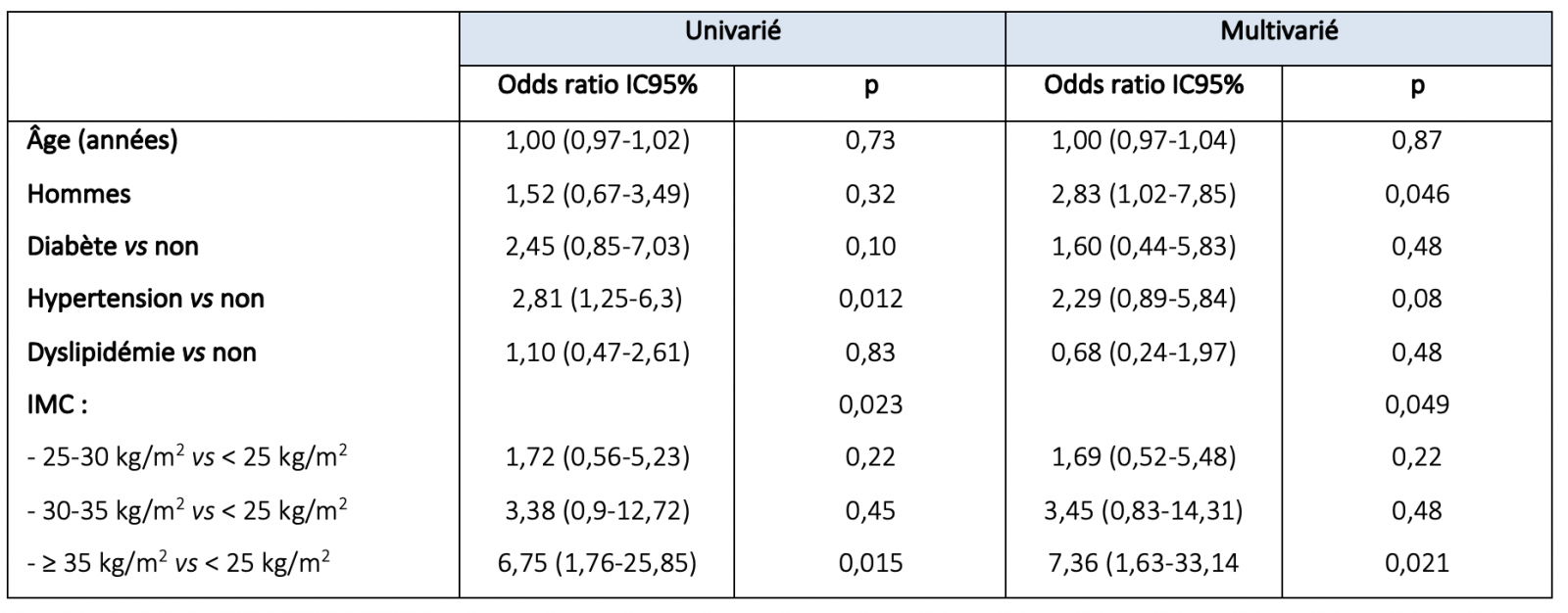
Une étude française monocentrique réalisée dans le service des soins intensifs du CHU de Lille a objectivé une association étroite entre l’obésité et les formes critiques de COVID-19 nécessitant le recours à la ventilation mécanique(18). Ces auteurs rapportent des fréquences d’obésité extrêmement élevées, IMC > 30 kg/m2 chez 47,6 % et > 35 kg/m2 chez 28,2 % (dont 14,5 % avec un IMC > 40 kg/m2) des 124 patients consécutifs admis en réanimation pour une pneumopathie à COVID-19 entre fin février et début avril 2020 (68,6 % ventilation mécanique). L’IMC > 30 kg/m2 était associé au recours à la ventilation mécanique, en analyse multivariée après ajustement sur l’âge, l’HTA et le diabète. Le risque relatif de recours à la ventilation mécanique était de 7,36 (IC95% : 1,63-33,14 ; p = 0,02) si l’IMC > 35 kg/m2 par rapport à un IMC < 25 kg/m2 (tableau 3).
L’obésité est reconnue comme un facteur de risque d’infection grave(19), comme illustré au cours de l’épidémie de grippe A H1N1, au cours de laquelle l’obésité a été décrite comme un facteur de prédisposition indépendant d’atteinte respiratoire grave(19,20). L’obésité abdominale est associée à une réduction de la ventilation de la base des poumons, entrainant une réduction de la saturation en oxygène dans le sang(21). L’obésité et le syndrome métabolique augmentent l’inflammation de type 2 qui peut avoir des effets délétères sur le parenchyme pulmonaire et les bronches(22). L’interleukine 6 (IL-6) est une protéine de l’inflammation, impliquée dans l’orage cytokinique suspecté d’être responsable de l’atteinte pulmonaire grave du COVID-19 avec SDRA(23,24), actuellement un des axes de recherche principaux avec les inhibiteurs de l’IL-6 (tels que le tozicizumab). Or, des taux élevés d’IL-6 ont été retrouvés chez des patients obèses et/ou porteurs d’un syndrome métabolique(25). Par ailleurs, la sécrétion anormale d’adipokines et de cytokines comme le TNF-alpha et l’interféron-gamma sont responsables d’une inflammation de bas grade chez les patients porteurs d’une obésité abdominale et pourraient être responsables d’une perturbation de la réponse immunitaire(19).
Ce lien entre l’obésité et la gravité de l’atteinte pulmonaire du COVID-19 doit amener, d’une part, à plus de vigilance avec les patients obèses pour éviter qu’ils ne contractent le COVID et, d’autre part, à une surveillance accrue des patients obèses testés positifs au COVID-19.
On parle beaucoup des autres facteurs de risque cardiovasculaire, mais les obèses semblent en fait plus à risque de déclarer une forme grave qu’un hypertendu ou un diabétique dont l’IMC ne dépasserait pas 25 kg/m2.
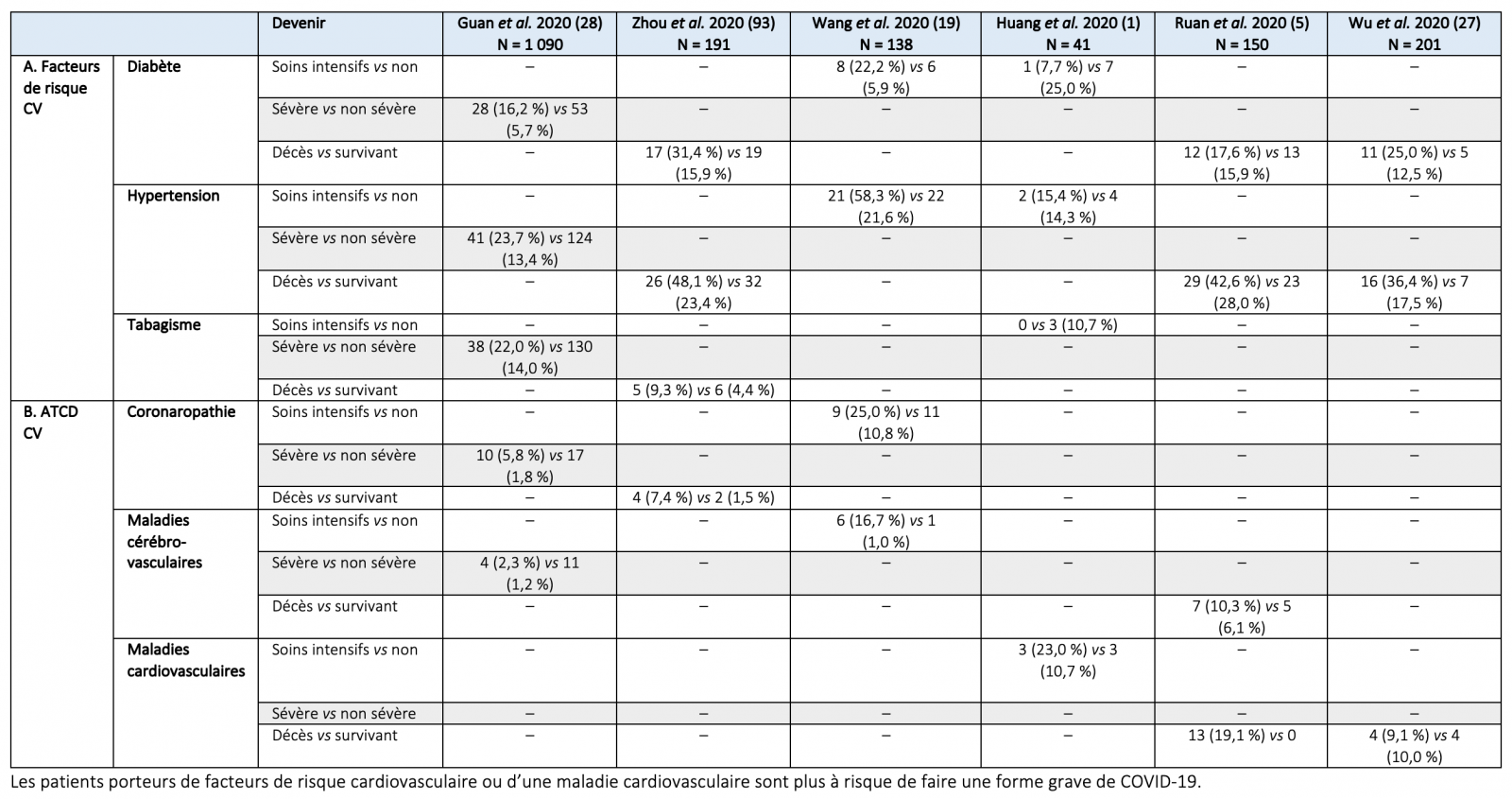
D’après Driggin E et al. Cardiovascular considerations for patients, health care workers, and health systems during the coronavirus disease 2019 (COVID-19) pandemic. JACC mars 2020
Figure 1. Interactions du SARS-CoV-2 et de l’ACE2, elle-même impliquée dans la contre-régulation du système rénine-angiotensine-aldostérone.
Lorsque le virus se lie à l’ACE2 à la surface de la cellule, le couple est internalisé, entrainant les effets pathogènes du virus. De plus, les propriétés protectrices de l’ACE2 chez l’individu sain, en inhibant le système rénine angiotensine aldostérone, sont diminuées, participant encore aux effets délétères observés de l’infection virale, notamment sur le système cardiovasculaire.
Tableau 3. Association entre les caractéristiques cliniques et le recours à la ventilation mécanique chez 125 patients COVID-19 admis en réanimation, en analyse uni- et multivariée.
D’après Simonnet A et al. High prevalence of obesity in severe acute respiratory syndrome coronavirus‐2 (SARS‐CoV‐2) requiring invasive mechanical ventilation. Obesity April 2020 Apr 9
Lorsque le virus se lie à l’ACE2 à la surface de la cellule, le couple est internalisé, entrainant les effets pathogènes du virus. De plus, les propriétés protectrices de l’ACE2 chez l’individu sain, en inhibant le système rénine angiotensine aldostérone, sont diminuées, participant encore aux effets délétères observés de l’infection virale, notamment sur le système cardiovasculaire.
Les atteintes cardiovasculaires associées au COVID-19
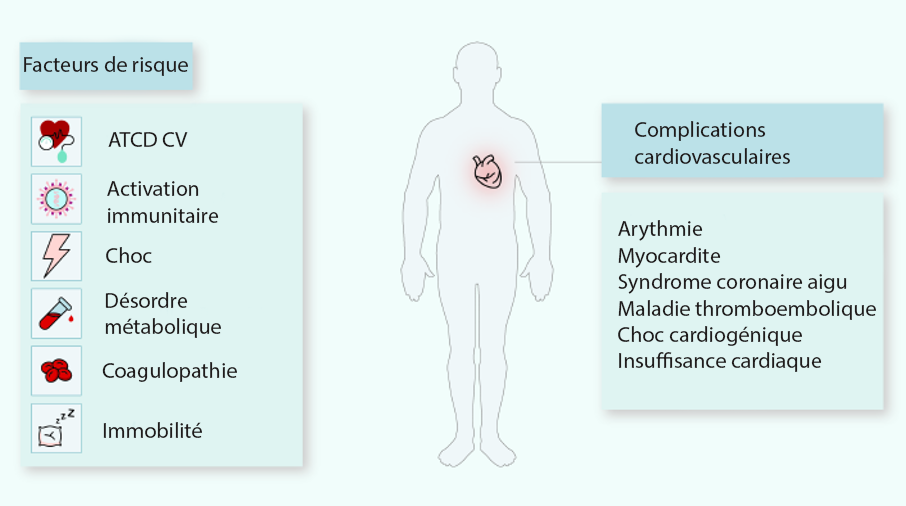
La figure 2 résume certaines des atteintes cardiovasculaires potentielles qui peuvent être associées au COVID-19. Dans l’attente d’études plus importantes, plusieurs articles suggèrent que l’infection par le SARS-CoV-2 entraînerait des complications cardiovasculaires ou la décompensation d’une maladie cardiovasculaire préexistante(6,15,29).
D’après Driggin E et al. Cardiovascular considerations for patients, health care workers, and health systems during the coronavirus disease 2019 (COVID-19) pandemic. JACC mars 2020
Figure 2. Facteurs de risque et complications cardiovasculaires potentielles du COVID-19.
Myocardites, souffrance myocardique et syndromes coronariens aigus
Les lésions myocardiques, traduites par une troponine positive, peuvent être dues à une ischémie myocardique ou à des processus non ischémiques incluant la myocardite(2,6,26). En cas de troubles respiratoires graves et d’hypoxie, en particulier en cas d’infection grave et de SDRA dus au COVID-19, il est possible que certains patients développent de telles lésions. Des taux élevés de troponine sérique ont été décrits chez de nombreux patients COVID-19, avec des taux significativement plus élevés chez les patients qui sont morts par rapport à ceux qui ont survécu(26). Dans une métaanalyse de 4 études comprenant un total de 341 patients COVID-19, la moyenne standardisée des niveaux de troponine I cardiaque était significativement plus élevée chez ceux présentant une forme grave de la maladie par rapport à ceux avec une forme non grave(27). Les niveaux de troponine peuvent être élevés chez les patients souffrant d’insuffisance rénale en raison d’une excrétion retardée.
Les tableaux de souffrance myocardique aiguë, qui comprennent non seulement une élévation des biomarqueurs mais aussi des anomalies à l’électrocardiogramme et à l’échocardiographie, sont très fréquents chez les patients COVID-19 et associés à un moins bon pronostic. Des études de cohortes chinoises de patients COVID-19 hospitalisés estiment que ces lésions surviennent chez 7 à 17 % des patients(28,30), et qu’elles sont nettement plus fréquentes chez les patients admis en soins intensifs (22,2 % contre 2,0 %, p < 0,001) et chez ceux qui sont décédés (59 % contre 1 %, p < 0,001)(2).
Des études antérieures sur d’autres coronavirus (MERS-CoV) ont objectivé des signes de myocardite par imagerie par résonance magnétique (IRM) cardiaque(29). Parmi les 68 patients décédés du COVID-19, 7 % ont été attribués à une myocardite avec choc cardiogénique et dans 33 % des cas la myocardite a été incriminée dans la mort du patient(26). D’autres ont décrit des myocardites fulminantes associées à une charge virale élevée, avec à l’autopsie des infiltrats mononucléés dans le tissu myocardique(30). L’atteinte péricardique n’a pas encore été décrite.
Il n’y a pas de donnée sur la survenue des syndromes coronariens aigus (SCA, infarctus de type 1) chez les patients COVID-19. L’activité inflammatoire importante et les variations hémodynamiques associées à une forme grave de COVID peuvent conférer un risque de rupture de la plaque d’athérome chez des patients à risque(2). L’étude de Kwong et coll.(31), en dehors du COVID-19, avait montré que les patients souffrant de troubles respiratoires aigus sont à haut risque de développer un infarctus du myocarde après une infection par le virus de la grippe (risque relatif à 6,1, IC95 % 3,9-9,5), ainsi qu’après des infections virales non grippales, y compris d’autres espèces de coronavirus (RR à 2,8, IC95% : 1,2-6,2). L’élaboration de parcours et de protocoles de soins spécifiques pour les patients COVID-19 atteints de STEMI est hautement souhaitable. Il est important de noter que le chevauchement est possible entre la symptomatologie d’un SCA et celle du COVID-19, comme décrit chez un patient italien souffrant de douleurs thoraciques et de modifications électrocardiographiques, avec une coronarographie normale, mais finalement un test positif au COVID-19(32). La prévalence réelle des SCA dans ce contexte peut être sous-estimée étant donné les problèmes liés à la disponibilité limitée des tests de dépistage et de l’accès à la coronarographie durant l’épidémie.
Zhou et coll.(2) ont retrouvé une insuffisance cardiaque chez 23,0 % des patients COVID-19, plus fréquente chez les patients décédés par rapport à ceux qui ont survécu (51,9 % contre 11,7 %). Le mécanisme précis de cette insuffisance cardiaque n’est pas connu : décompensation d’une dysfonction ventriculaire gauche préexistante ou atteinte aiguë de novo, myocardite, cardiomyopathie de stress (comme décrit avec le virus de la grippe)(32). Les premiers cas de myocardites à COVID(33) et de syndromes de Tako-Tsubo (myocardite de stress) ont été décrits(34,35), sans qu’il soit possible d’en estimer la réelle prévalence. L’insuffisance cardiaque droite et l’hypertension artérielle pulmonaire sont possibles dans le contexte de maladie pulmonaire parenchymateuse et de SDRA.
Arythmies
L’arythmie est une manifestation cardiaque décrite chez les patients COVID-19. Bien que non spécifiques, les palpitations étaient présentes chez 7,3 % des patients d’une cohorte de 137 patients COVID-19(36). Dans une cohorte chinoise de 138 patients COVID-19 hospitalisés, une arythmie constatée chez 16,7 % des patients, et était plus fréquente chez les patients en unité de soins intensifs (44,4 % contre 6,9 %)(37). Les spécificités des types d’arythmies n’ont pas encore été publiées. La forte prévalence de l’arythmie pourrait être en partie attribuable aux désordres métaboliques, à l’hypoxie, au stress neuro-hormonal ou inflammatoire dans le cadre de cette infection virale. Toutefois, l’apparition d’une tachyarythmie maligne dans un contexte d’élévation de la troponine doit faire suspecter une myocardite sous-jacente.
Choc cardiogénique et choc mixte
La présentation clinique la plus fréquente du COVID-19 est une atteinte respiratoire aiguë pouvant conduire à un SDRA, se manifestant par des opacités en verre dépoli sur l’imagerie thoracique et une hypoxémie. Des caractéristiques similaires peuvent être observées dans le cas d’œdème pulmonaire d’origine cardiogénique, de novo ou préexistant. Il est donc important de considérer comme d’origine cardiogénique ou mixte (cardiaque et pulmonaire) les manifestations respiratoires du COVID-19. Historiquement, le cathétérisme droit a été utilisé pour mesurer la pression capillaire pulmonaire afin de faciliter cette distinction ; mais la pression artérielle pulmonaire a été retirée des critères de Berlin utilisés pour le diagnostic de SDRA. Ces critères utilisent plutôt le délai depuis le début des symptômes, l’imagerie avec des opacités pulmonaires bilatérales et l’absence de surcharge volumique pour faire le diagnostic de SDRA(38). Dans de nombreux cas, le BNP et l’échocardiographie peuvent aider à clarifier le diagnostic. Si ces tests ne permettent pas de trancher sur la part pulmonaire et cardiogénique, le cathétérisme de l’artère pulmonaire peut être envisagé pour évaluer les pressions de remplissage, le débit cardiaque, et guider la prise de décision, sachant l’approche thérapeutique très différente pour le SDRA et le choc cardiogénique. Il est crucial de déterminer si une composante cardiogénique concomitante est présente avant la mise en place d’un support mécanique respiratoire ou circulatoire (ECMO), car le choix du dispositif peut être différent (ECMO veino-veineuse vs veino-artérielle). Dans les infections les plus sévères avec SDRA et pneumonies nécrosantes, le pronostic du patient peut être très péjoratif même avec le support d’une ECMO. Dans une série de cas de 52 patients avec une atteinte grave de COVID-19, 5 des 6 patients qui ont bénéficié d’une ECMO n’ont pas survécu. Des études complémentaires sont nécessaires, pour évaluer l’utilité de l’ECMO dans les atteintes graves du COVID-19(39).
Le cas particulier de la transplantation cardiaque
Lors d’épidémies antérieures de coronavirus (SARS-CoV-1 et MERS-CoV), les patients greffés ayant contracté le virus présentaient des symptômes similaires à ceux de la population générale(40). Dans la pandémie actuelle, deux greffés cardiaques COVID-19 de la province chinoise du Hubei présentaient de la fièvre et leurs bilans biologiques et scanners thoraciques étaient semblables à ceux des patients non immunodéprimés(41). L’un avait une maladie relativement bénigne prise en charge en ambulatoire, l’autre a dû être hospitalisé pour une oxygénothérapie ne nécessitant pas de soins intensifs. Les deux ont survécu et ont été traités avec des antibiotiques et des antiviraux, le plus sévère des deux ayant également arrêté son traitement immunosuppresseur et reçu des corticoïdes et des Ig IV. Une enquête menée auprès de 87 greffés cardiaques à Wuhan n’a pas trouvé de risque plus élevé d’infection par le SARS-CoV-2 si les mesures préventives de routine étaient utilisées(42). Bien qu’elle soit encourageante, cette notion doit être confirmée sur des populations plus importantes.
Faut-il continuer les transplantations cardiaques en raison du risque d’exposition au SARS-CoV-2 pendant l’hospitalisation, et de l’inquiétude concernant le contrôle de l’infection chez ces patients immunodéprimés ? Il n’existe pas de recommandations des sociétés savantes, mais les équipes de transplantation conseillent de poursuivre la transplantation cardiaque sans modification du traitement immunosuppresseur, à condition que le receveur n’ait pas été testé positif pour le SARS-CoV-2 et qu’il n’ait pas été exposé ou n’en ait pas présenté les symptômes au cours des deux à quatre semaines précédentes. Il faut éviter les donneurs dont l’atteinte par le COVID-19 est connue ou suspectée, par analogie avec l’attitude préconisée lors de l’épidémie grippe H1N1(43). Si un donneur a eu le COVID-19, la recherche de SARS-CoV-2 par PCR doit être négative pendant au moins 14 jours (en raison de la période d’incubation d’environ 5 jours et de l’apparition des symptômes en 11,5 jours en moyenne). Les difficultés de cette décision reposent sur la prévalence croissante de l’infection à SARS-CoV-2 chez les donneurs qui peuvent être asymptomatiques (18 % à 30 %), surtout si le donneur ne peut pas être testé. Les recommandations sur la gestion des receveurs de greffe qui ont développé un COVID-19, basée sur des données limitées à ce jour, sont la poursuite de l’immunosuppression pour les formes non graves avec réduction de la dose de l’anti-métabolite (mycophénolate ou azathioprine) et ajout d’un traitement complémentaire (antiviral, corticothérapie) en fonction de la gravité de la maladie. Il faut faire attention aux interactions médicamenteuses, notamment avec les inhibiteurs de protéase, qui sont une option de traitement à l’essai pour les COVID-19 et qui vont augmenter les taux d’anti-calcineurine.
Médicaments et COVID-19 : interactions et implications cardiovasculaires
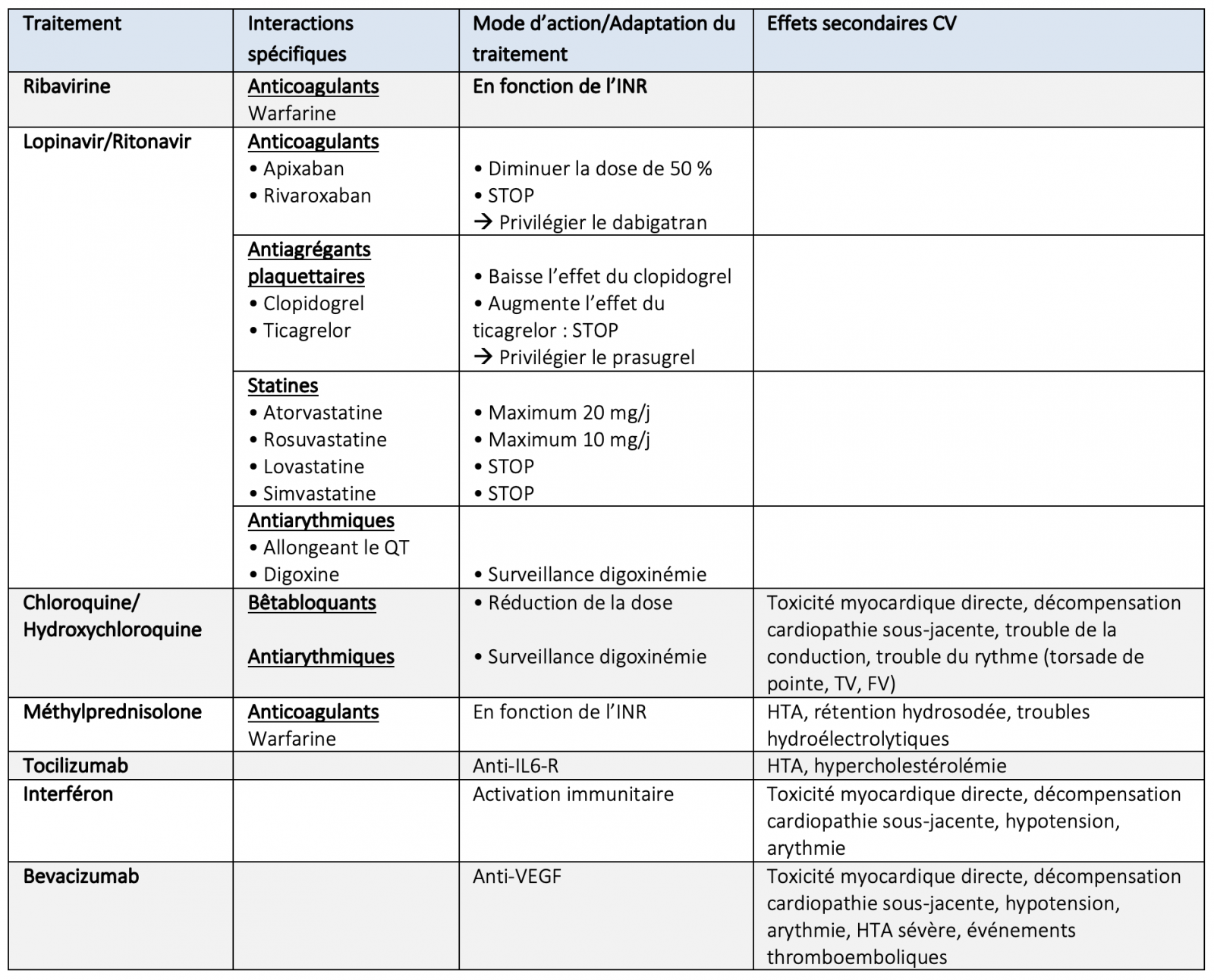
Les données concernant les thérapies antivirales et autres stratégies de traitement, ainsi que leurs potentielles interactions avec les médicaments CV et les toxicités CV sont résumées dans le tableau 4.
Tableau 4. Traitements du COVID-19, interactions avec les traitements à visée cardiovasculaire et effets secondaires cardiovasculaires potentiels.
• Médicaments antiviraux
La ribavirine et le remdesivir sont deux agents qui se lient au site actif sur l’ARN polymérase ARN-dépendante du SARS-CoV-2(44). Le lopinavir/ritonavir inhibe la réplication du virus à ARN et a un effet synergique in vitro avec la ribavirine(45). La ribavirine et le lopinavir/ritonavir sont à l’étude dans le cadre d’essais cliniques pour le COVID-19 et ont été utilisés pendant des années comme éléments de traitement de l’hépatite C et du VIH. Alors que la ribavirine n’a pas de toxicité CV directe caractérisée, le lopinavir/ritonavir peut entraîner un allongement de l’intervalle QT et de l’espace PR, en particulier chez les patients qui présentent un QT long de base ou ceux qui sont à risque de trouble conductif, y compris ceux qui prennent d’autres médicaments allongeant le QT. La ribavirine et le lopinavir/ritonavir peuvent modifier l’effet des anticoagulants: la ribavirine a des effets variables sur le dosage de la warfarine(46) et le lopinavir/ritonavir a des effets sur les anticoagulants oraux directs (tels que le rivaroxaban et l’apixaban). Les inhibiteurs de l’HMG-CoA réductase (statines) peuvent interagir avec la combinaison lopinavir/ritonavir et entraîner une myopathie due à des taux élevés de statines lorsqu’ils sont administrés ensemble. La lovastatine et la simvastatine en particulier sont contre-indiquées en cas de co-administration avec le lopinavir/ritonavir en raison du risque de rhabdomyolyse. Les autres statines, y compris l’atorvastatine et la rosuvastatine, doivent être administrées à la dose la plus faible possible.
• Autres traitements
La chloroquine (agent antipaludéen) ou l’hydroxychloroquine (utilisée dans les maladies auto-immunes) sont utilisées depuis des décennies, et bloquent la réplication du SARS-CoV-2 en augmentant le pH endosomal requis pour la fusion virus/cellules. Elles ont in vitro une activité inhibitrice sur le SARS-CoV-2(47,48). La chloroquine et les substances étroitement apparentées (l’hydroxychloroquine) ont un potentiel de toxicité myocardique intermédiaire retardée. Les facteurs de risque sont l’exposition à long terme (> 3 mois), une dose élevée en fonction du poids, une maladie cardiaque préexistante, et une insuffisance rénale. La toxicité cardiaque de la chloroquine se présente sous la forme d’une cardiomyopathie restrictive ou dilatée, ou des troubles de conduction. Enfin, les deux sont associés à un risque de torsade de pointe chez les patients avec des troubles ioniques ou en cas d’utilisation concomitante d’agents allongeant l’intervalle QT. L’exposition à court terme à ces agents, comme attendue dans le traitement du COVID-19, confère un risque plus faible de ces effets secondaires essentiellement dépendants de la dose et de la durée du traitement.
La méthylprednisolone est actuellement utilisée dans le traitement des formes graves de COVID-19 compliqués de SDRA. Ce corticostéroïde est connu pour provoquer une rétention hydrosodée et de l’hypertension comme effets CV directs, et peut également interagir avec la warfarine via un mécanisme non connu.
Enfin, la détérioration de l’état clinique du patient présentant une forme grave de COVID-19 peut poser des difficultés pour l’administration des médicaments à visée cardiovasculaire, allant du traitement antiplaquettaire aux bêtabloquants, rendant les patients atteints ou à risque de cardiopathie ischémique ou d’insuffisance cardiaque plus à risque de décompenser.
• Inhibiteurs de l’angioconvertase (IEC) et inhibiteurs des antagonistes des récepteurs ATR-1 de l’angiotensine 2 (ARAII)
L’angioconvertase de type 2 (ACE2) est une enzyme impliquée dans la contre-régulation du système rénine-angiotensine-aldostérone (SRAA). Ses effets sont à ce titre bénéfiques (vasodilatation, anti-inflammatoire, antifibrotique) contre balançant les effets potentiellement néfastes du SRAA (vasoconstriction, inflammation, augmentation de la pression artérielle)(49). L’ACE2, en plus d’être une enzyme, est le récepteur transmembranaire utilisé par le SARS-CoV-2 pour pénétrer par endocytose dans les cellules hôtes(4). L’effet des IEC et des ARAII sur cette enzyme/récepteur est incomplètement connu. Certaines données suggèrent que les IEC et les ARAII pourraient réguler l’ACE2 à la hausse, facilitant la pénétration du virus dans la cellule hôte (figure 1)(50). D’autres études suggèrent que les IEC et ARAII pourraient potentialiser la fonction de protection pulmonaire de l’ACE2 en tant qu’inhibiteur de l’angiotensine 2(51-53). En fait, le rôle de l’ACE2 au cours de l’infection à SARS-CoV-2 apparaît complexe : d’un côté plutôt bénéfique en régulant à la baisse le SRAA, d’un autre côté délétère en rendant le système pulmonaire et cardiovasculaire plus sensibles au virus en servant de corécepteur d’entrée cellulaire. Malgré le manque de preuve clinique, il y a eu débat sur la nécessité de poursuivre ou d’arrêter les IEC/ARAII chez les patients hypertendus et COVID-19. Ces éléments ont pu semer le trouble chez les patients (sollicitant des changements dans leur traitement antihypertenseur), et une incertitude croissante des médecins. En réponse, le Conseil de l’hypertension de la Société européenne de cardiologie, et la plupart des sociétés savantes internationales, recommandent aux médecins et aux patients de poursuivre le traitement avec leurs antihypertenseurs habituels, car il n’y a aucune preuve clinique ou scientifique suggérant que le traitement par IEC/ARAII soit délétère. Pour les patients les plus graves, en état de choc, la poursuite ou l’arrêt des IEC/ARAII reste à la discrétion du médecin en charge du patient en soins intensifs(54). La communauté scientifique devra mieux décrire le rôle du SRAA et spécifiquement de l’ACE2 dans la pathogenèse du COVID-19, tandis que les données cliniques accumulées et une étude française prospective randomisée en cours (ACORES 2) devraient permettre de déterminer s’il existe un lien entre IEC/ARAII et la morbi-mortalité liée au COVID-19.
Gestion du risque pour les patients, le personnel soignant, et le suivi des patients COVID et non-COVID
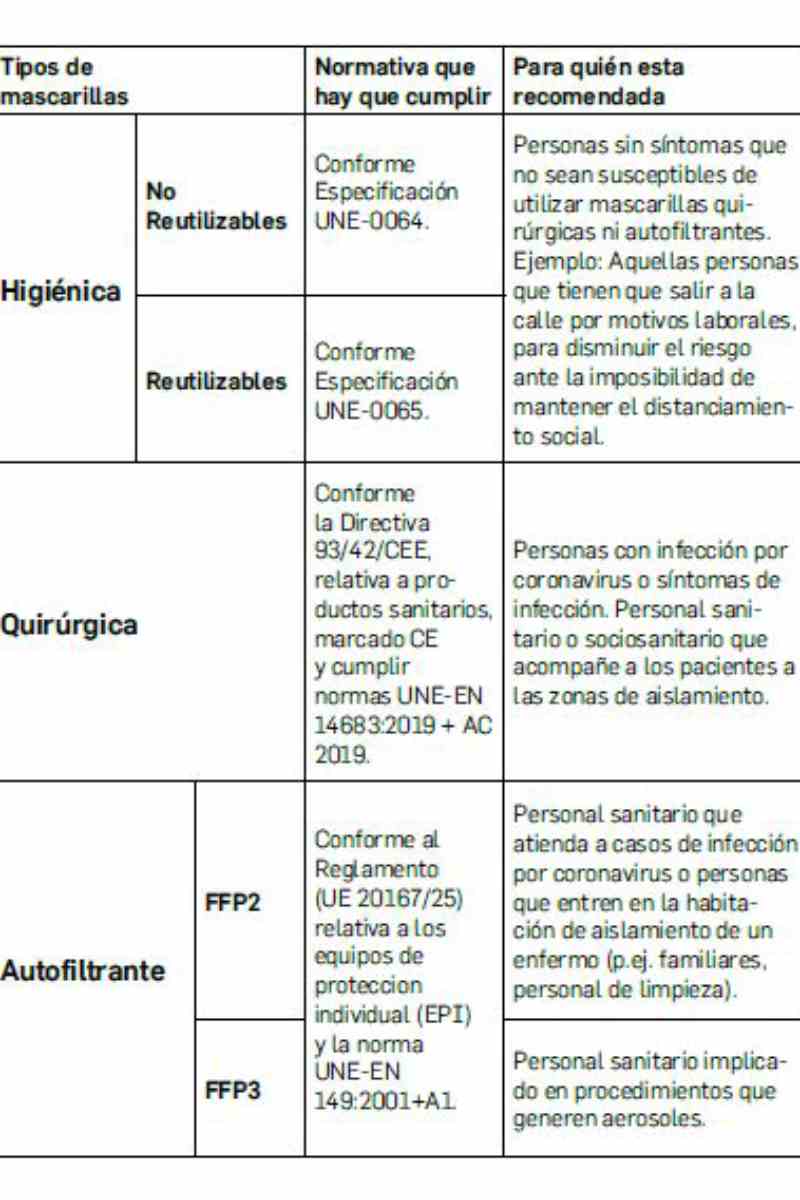
Équipements de protection pour le personnel soignant
Les premières données ont suggéré que la transmission du SARS-CoV-2 se fait le plus souvent par des gouttelettes respiratoires produites lorsqu’une personne infectée tousse ou éternue. Ces gouttelettes peuvent se déposer sur le mucus ou être inhalées dans les poumons de ceux qui se trouvent à proximité. Le virus peut rester actif sur des surfaces inertes pendant plusieurs jours(55). Lors de l’exécution de certaines procédures qui génèrent des aérosols, telles que l’échocardiographie transœsophagienne, l’intubation endotrachéale, et la réanimation cardio-pulmonaire, des équipements de protection individuelle supplémentaires peuvent être nécessaires. Des mesures de prévention et de contrôle des infections spécifiques à la cardiologie interventionnelle doivent être mises en place. En cas d’arrêt cardiaque, les manœuvres de réanimation cardio-pulmonaire provoquant la diffusion de particules virales, exposent à une contamination des professionnels de santé et des autres patients.
Le nettoyage de tous les équipements potentiellement contaminés par le SARS-CoV-2 est indispensable.
Le temps d’arrêt nécessaire pour le nettoyage peut avoir un impact important sur la disponibilité du laboratoire de cathétérisme. Ainsi, de nombreux hôpitaux ont annulé les procédures facultatives pendant la phase de croissance de l’épidémie. Les soignants sont à très haut risque de contracter le virus, comme démontré par Wu et coll., notant que 1 716/44 672 (3,8 %) personnes infectées étaient du personnel de santé(6). Cela implique de limiter l’activité les explorations CV aux indications urgentes, et d’annuler tout l’activité programmée non urgente (maladie coronaire stable, ischémie silencieuse, bilan d’HTA, bilan de valvulopathie asymptomatique…).
• Organisation du suivi des patients avec maladies cardiovasculaires
De nombreuses mesures spécifiques doivent être prises pour la prise en charge des patients CV afin de minimiser le risque de transmission de COVID-19 aux patients et au personnel de santé, notamment la télémédecine. Celle-ci apparaît idéale en cas de crise de santé publique car elle permet de trier les patients tout en réduisant au minimum l’exposition des patients et du personnel de santé à une infection potentielle. L’éducation des patients est essentielle pour respecter les consignes de quarantaine en cas de survenue de symptômes de COVID non grave. Les services doivent disposer d’équipements de protection individuels en quantité suffisante pour le personnel et les patients.
• Prise en charge des infarctus du myocarde
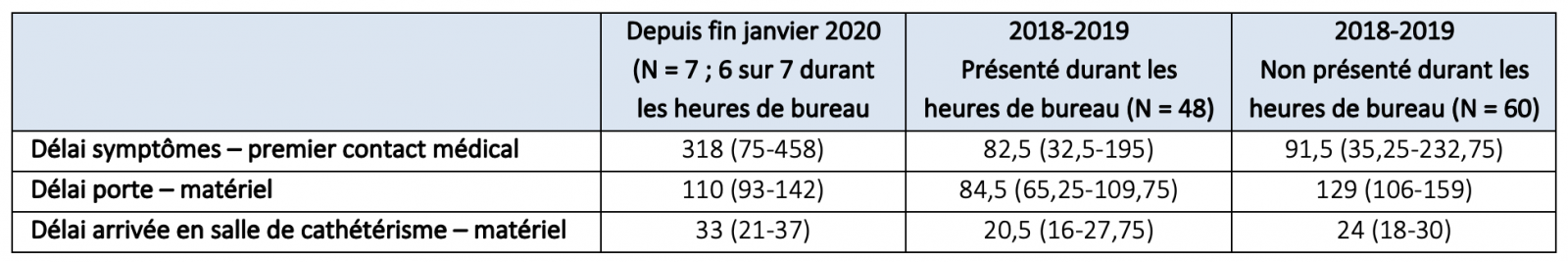
La crise du COVID-19 semble aboutir à une surmortalité cardiovasculaire, en partie expliquée par un retard dans la prise en charge des syndromes coronariens aigus. Chor-Cheung et coll.(56) ont rapporté à Hong Kong un délai multiplié par 4 dans la prise en charge des infarctus (tableau 5). La mortalité indirecte de l’épidémie peut être due aux réticences des patients à fréquenter les hôpitaux en période COVID-19 et donc à des appels plus tardifs, ainsi qu’à un allongement du délai de prise en charge (transport avec mesures de protection) puis une fois admis à l’hôpital (habillage du personnel, nettoyage de la salle…).
Tableau 5. Délais de prise en charge des STEMI avant et après la crise du COVID-19 dans un centre hospitalier de Hong Kong.
D’après Chor-Cheung et al. Impact of coronavirus disease 2019 (COVID-19) outbreak on ST-segment–Elevation myocardial infarction care in Hong Kong, China. Circ Cardiovasc Qual Outcomes April 2020
EN PRATIQUE
• Le COVID-19 peut avoir des impacts cardiovasculaires multiples, directs et indirects (y compris sur la prise en charge des patients COVID-19 négatifs).
• Les facteurs de risque cardiovasculaire ne semblent pas surreprésentés chez les patients COVID-19 par rapport à la population générale. En revanche, les facteurs de risque cardiovasculaire, y compris un antécédent de MCV, sont associés à une surmortalité au cours du COVID-19.
• Une grande vigilance s’impose avec les patients obèses particulièrement exposés aux formes graves de COVID-19 (plus qu’un hypertendu ou un diabétique dont l’IMC ne dépasse pas 25 kg/m2).
• Des efforts concertés des professionnels de santé et d’une direction incisive sont nécessaires pour atténuer le risque sanitaire pour la population générale et pour les professionnels de santé eux-mêmes.
• La mise à profit des capacités de télésanté et le respect optimal des mesures de prévention à l’échelle de la population devraient nous permettre de passer cette période jusqu’à ce que l’épidémie régresse.
Références sur demande à la rédaction : biblio@axis-sante.com